

2021年1月19日,,美國食品藥品管理局(FDA)宣布其為新型煙草制品完善了上市前審查的兩項基本規(guī)則,,即,,規(guī)定了有關(guān)煙草制品上市前申請(Premarket Tobacco Product Applications, PMTAs)及實質(zhì)性等同原則(Substantial Equivalence, SE)報告的內(nèi)容,、格式和審查的最低要求等相關(guān)信息,。制造商可通過FDA的PMTAs和SE這兩種途徑獲取新型煙草制品銷售許可。
據(jù)FDA介紹,,新型煙草制品PMTA和SE報告等規(guī)則的相關(guān)內(nèi)容如下:
(1)PMTA最終規(guī)則
PMTA是所有新型煙草制品獲得FDA銷售許可的一種申請,。FDA要求任何電子尼古丁遞送系統(tǒng)(ENDS)產(chǎn)品的上市前申請需要通過PMTA途徑提交。
在PMTA途徑下,,制造商或進(jìn)口商需向FDA機(jī)構(gòu)進(jìn)行論證其煙草制品上市符合公共健康保護(hù)的要求,。FDA對煙草制品評估包括對成分、原料,、添加劑,、結(jié)構(gòu)、毒理學(xué)特征和對健康影響的審查,,以及產(chǎn)品的制造,、包裝和標(biāo)簽方式、消費者感知研究(如有)以及申請人對產(chǎn)品營銷計劃的描述,。
PMTA最終規(guī)則將確保這些申請包含足夠的信息以供FDA評估,,包括有關(guān)煙草制品物理特征的詳細(xì)信息以及有關(guān)該產(chǎn)品潛在的公共健康風(fēng)險的信息。最終規(guī)則描述了申請人必須在PMTA中包含的信息,,以便FDA完成對申請的實質(zhì)性審查,。它還正式確定了FDA在審查PMTA時將遵循的程序,以及對收到上市許可的申請人的上市后報告要求,。最終規(guī)則還要求煙草制品制造商保留其煙草制品合法銷售的記錄,,例如展示煙草制品進(jìn)行上市前無需審查或取得上市前授權(quán)的相關(guān)文件。
除了內(nèi)容和格式要求外,,最終規(guī)則還規(guī)定了FDA在評估PMTA時遵循的一般程序,,包括申請接受、申請備案和檢查,。最終規(guī)則也對其他PMTA相關(guān)要求進(jìn)行了描述,,包括提交申請修訂、審查時間,、撤回申請,、所有權(quán)變更、上市后報告,、記錄維護(hù),、FDA與申請人的通信方式、FDA的審查結(jié)果披露程序和電子提交相關(guān)要求,。最終規(guī)則還解釋了申請人如何提交補(bǔ)充PMTA或重新提交的方式,。
FDA在2019年9月20日發(fā)布了法規(guī)草案征求公眾意見,,在收到公眾意見并進(jìn)行審查后,確定了最終規(guī)則,。最終規(guī)則發(fā)布后,,F(xiàn)DA將撤回其2011年9月的指南草案,因在最終規(guī)則已涉及其主題,。
(2)SE最終規(guī)則
FDA期望SE可成為卷煙,、無煙煙草、雪茄,、水煙煙草和自用卷煙煙草申請上市最常用的途徑。
為了確定一款新的煙草制品實質(zhì)等效,,F(xiàn)DA必須確定其與已過審上市的煙草制品(predicate tobacco product)具有相同的特征,,或者與已過審上市的煙草制品具有不同的特征,但該特征不會引起各類公眾健康問題,。
SE最終規(guī)則提供了有關(guān)SE報告內(nèi)容和格式最低要求的附加信息,,從而為所有利益相關(guān)者提供了更高的可預(yù)測性和效率。有助于確保SE報告包含足夠的信息供FDA對新型煙草制品與已過審上市的煙草制品之間的評估比較,。
最終規(guī)則還涉及以下內(nèi)容:FDA與申請人的通信,、支持SE報告的存檔、SE報告的保密性,、申請人如何修改或撤回SE報告,、申請人如何將SE報告的所有權(quán)轉(zhuǎn)讓給新的申請人、SE報告電子方式提交和修訂,。
(3)其他
這兩項最終規(guī)則均將在《聯(lián)邦紀(jì)事》上發(fā)布后30天生效,。FDA將繼續(xù)為MRTP申請制定單獨的規(guī)則,此規(guī)則將為那些尋求將煙草制品作為改良或低風(fēng)險產(chǎn)品進(jìn)行營銷的人提供詳細(xì)信息,,包括如何組織和提交MRTP申請,。
由于2016年8月8日后上市的被認(rèn)定為新型煙草制品(包括電子煙產(chǎn)品)的制造商必須在2020年9月9日前向FDA提交上市前申請,F(xiàn)DA正在處理收到的大量申請,,并已開始了審查流程,。FDA將在接下來的幾周里提供一份自2020年9月9日截止日期以來,該進(jìn)程內(nèi)容的更加詳細(xì)的更新,。
本新聞由廣東省WTO/TBT通報咨詢研究中心摘錄/編輯/整理并翻譯,,轉(zhuǎn)載請注明來源。
更多詳情請見:
https://www.fda.gov/news-events/press-announcements/fda-marks-historic-public-health-milestone-finalization-two-key-rules-companies-seeking-market-new
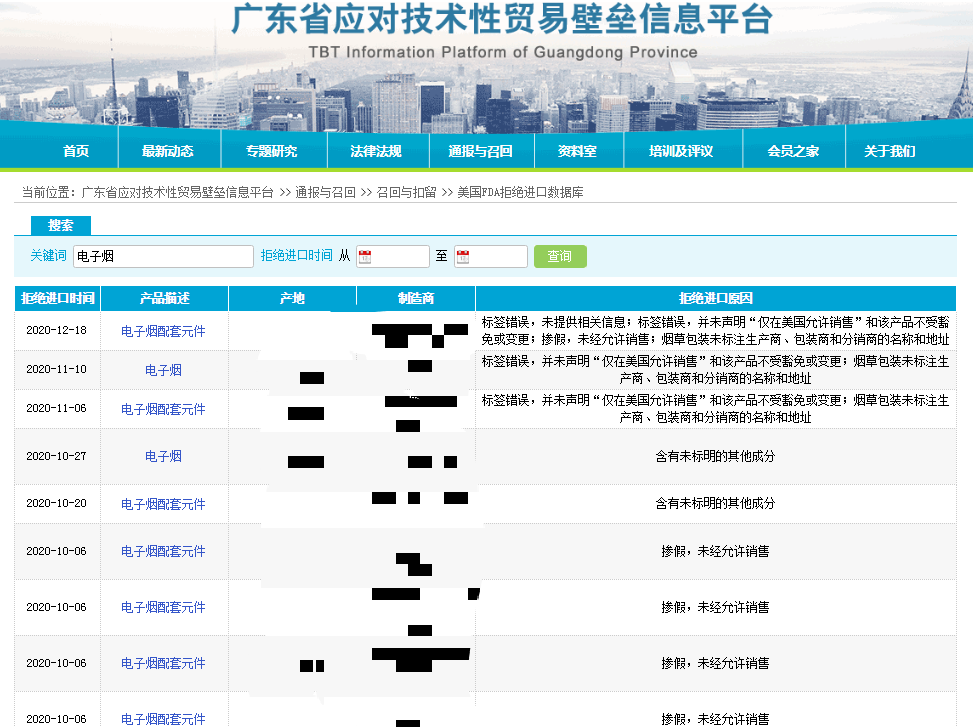
*據(jù)不完全統(tǒng)計,,2020年中國被美國FDA拒絕進(jìn)口的電子煙及配套產(chǎn)品超過200例,,廣東省WTO/TBT通報咨詢研究中心在此提醒相關(guān)出口企業(yè)加強(qiáng)對上述規(guī)則的關(guān)注。

關(guān)注“廣東技術(shù)性貿(mào)易措施”,,獲取更多服務(wù),。
